导读:在细胞治疗、生物制药、日常科研及临床诊断领域,支原体污染被称为“隐形杀手”,其检测是保障安全的关键环节。而检测的准确性,往往取决于第一步——基因组DNA的提取效率。面对微量、复杂基质的样本,如何快速、高效地提取出高纯度的支原体基因组DNA,筑牢细胞质控的关键基石?今天,我们从原理到实践,全方位解析一款专为支原体打造的离心柱法基因组DNA提取试剂盒。
01 痛点直击:支原体DNA提取的三大“拦路虎”
支原体(Mycoplasma)是一类无细胞壁的最小原核微生物,其体积微小(0.2-0.3 μm),常隐匿于细胞培养上清或生物制品深处。据统计,全球约15%-35%的细胞培养物存在支原体污染[1],而支原体污染会导致细胞生长速率改变、代谢途径干扰、实验数据失真,还可能引发染色体畸变,严重影响生物制品的有效性与安全性。因此,建立快速、高灵敏度的检测机制是确保细胞与生物制品真实性及安全性的绝对前提。
目前,支原体检测方法主要包括三类:传统培养法、核酸扩增(NAT)法和指示细胞培养法。其中,NAT法因其快速、灵敏的特点日益受到青睐,但无论采用何种分子生物学检测方法,高质量DNA模板的获取都是决定检测结果可信度的关键因素。
在DNA提取环节,科研人员常面临三大“拦路虎”:
1. 起始量极低:污染早期,样本中支原体拷贝数可能低至个位数。根据欧洲药典(EP 2.6.7) 要求,NAT检测方法必须具备极高的灵敏度以检出低载量污染,传统方法回收率低,极易导致假阴性 [2-3]。
√本公司解决方案:采用高效核酸富集技术与超灵敏扩增体系,检测灵敏度可达10 CFU/mL,完全符合欧洲药典(EP 2.6.7) 标准,彻底消除低载量假阴性风险。
2. 抑制剂干扰:细胞培养液中的蛋白、血清、抗生素,以及生物制品中的辅料(如人血白蛋白),常残留于提取物中。这些物质是Taq DNA聚合酶的强效抑制剂,可直接导致PCR反应失败[4]。
√本公司解决方案:内置强效杂质去除模块与高耐受性酶系,能特异性吸附核酸并有效抵抗蛋白、血清及抗生素抑制,确保复杂基质样本扩增零失败。
3. 操作繁琐有毒性:传统酚氯仿法毒性大、步骤多;普通通用型试剂盒未针对支原体优化,裂解不彻底。
√本公司解决方案:摒弃有毒酚氯仿,提供针对支原体优化的无毒快速裂解方案;全程仅需40分钟,步骤简便且大幅增加安全性能,提升检测效率。
“提取失败,检测白费。”因此,选择一款高灵敏度、高纯度的专用提取试剂盒,是确保支原体检测(尤其是NAT法)准确性的基石。
02 原理深究:离心柱法DNA提取核心机制解析
离心柱法利用特殊的硅胶膜吸附柱,在高盐及离液剂的存在下破坏核酸水化层,DNA通过阳离子桥接、脱水效应以及氢键等多种作用力与硅胶表面的硅醇基发生相互作用,从而实现选择性吸附[5]。而在低盐高pH条件下,这些作用力被破坏,DNA被洗脱。
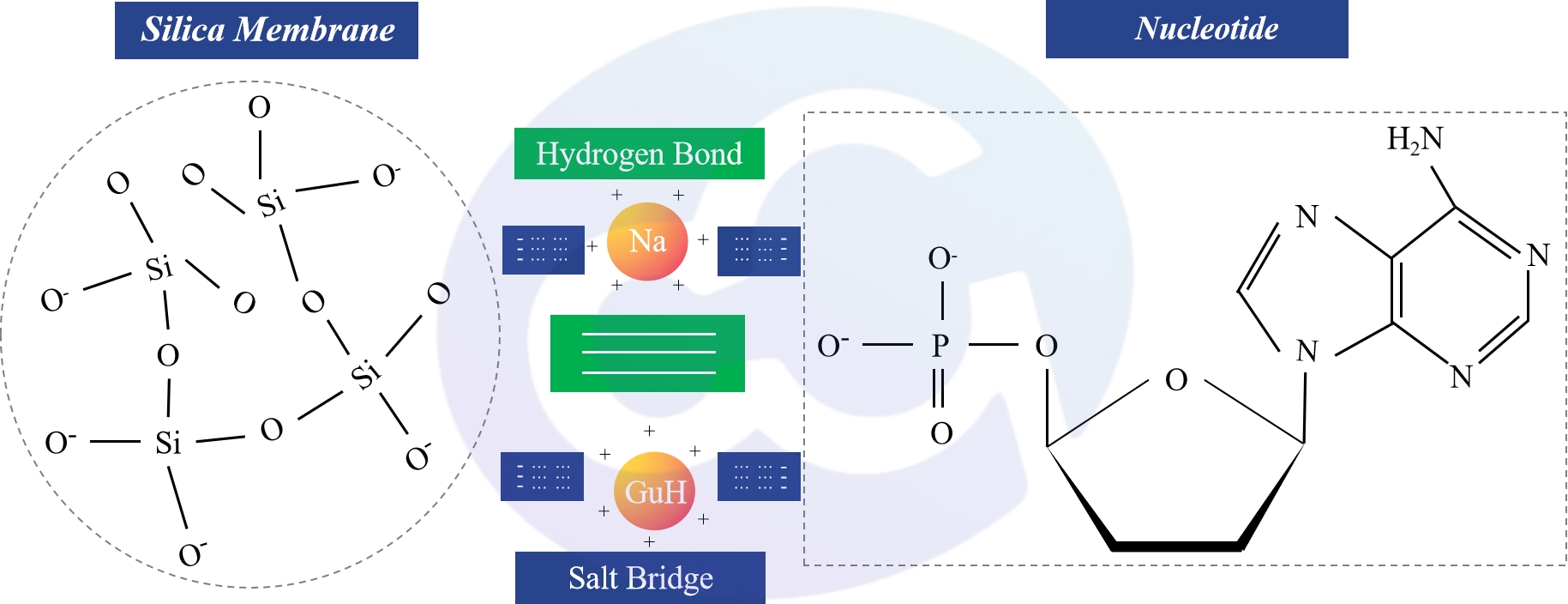 图2-1 硅胶膜结合核酸机制
图2-1 硅胶膜结合核酸机制
其核心流程包含四个关键步骤:
(1)裂解 (Lysis)
加入裂解液,彻底破坏支原体独特的无细胞壁结构并释放基因组DNA。
(2)柱结合 (Column Binding)
加入结合液调节环境,使释放出的支原体DNA特异性地吸附在离心柱的硅胶膜上。
(3)洗涤 (Washing)
使用洗涤液冲洗离心柱,去除残留的蛋白质、脂质及培养液杂质,同时保留DNA。
(4)洗脱 (Elution)
向离心柱膜中央加入洗脱液,将纯净的支原体DNA溶解并收集到管中。
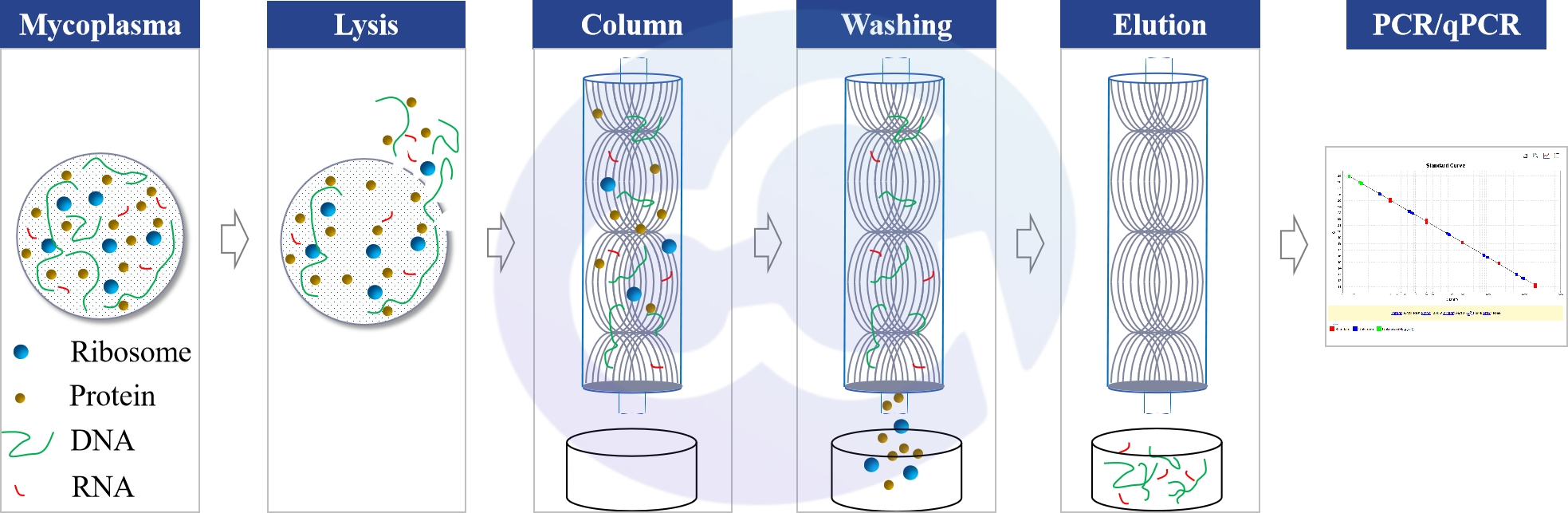 图2-2 离心柱法DNA提取试剂盒核心流程
图2-2 离心柱法DNA提取试剂盒核心流程
03 深度横评:六大提取方法大比拼
3.1 机理与利弊分析
在核酸提取领域,技术路线的选择直接决定实验成败。目前常用的基因组DNA提取方法主要包括:离心柱法、磁珠法、酚-氯仿法、碱裂解法、煮沸裂解法、Chelex-100法等。
_Sheet2.jpg)
对于支原体检测这一对灵敏度和纯度要求极高的应用场景,离心柱法在成本、性能与操作灵活性之间取得了最佳平衡,是目前大多数实验室的首选,尤其适合未配备全自动核酸提取仪的中小型QC实验室[6]。
3.2 不同方法样本实测
为验证不同提取方法在支原体样本中的综合性能,本研究选取了具有代表性的支原体菌株、细胞、细胞上清样本,严格控制相同起始量与检测条件,平行对比了离心柱法、磁珠法及碱裂解法,重点评估了各方法在核酸得率、纯度(A260/A280)、qPCR应用中的差异。
表3-1 10 CFU口腔支原体
|
抽提方法 |
浓度 |
A260/A280 |
CT值 |
|
离心柱法 |
3.9 |
1.87 |
31.65 |
|
磁珠法 |
2.0 |
1.98 |
32.87 |
|
碱裂解法 |
32.5 |
1.55 |
36.05 |
表3-2 10 CFU猪鼻支原体
|
抽提方法 |
浓度 |
A260/A280 |
CT值 |
|
离心柱法 |
2.5 |
1.74 |
32.36 |
|
磁珠法 |
2.1 |
1.77 |
35.51 |
表3-3 BHK细胞上清
|
抽提方法 |
浓度 |
A260/A280 |
CT值 |
|
离心柱法 |
13.5 |
1.86 |
18.61 |
|
碱裂解法 |
229.3 |
1.14 |
21.50 |
表3-4 BHK细胞
|
抽提方法 |
浓度 |
A260/A280 |
CT值 |
|
离心柱法 |
28.8 |
1.83 |
16.20 |
|
碱裂解法 |
66.9 |
1.57 |
16.87 |
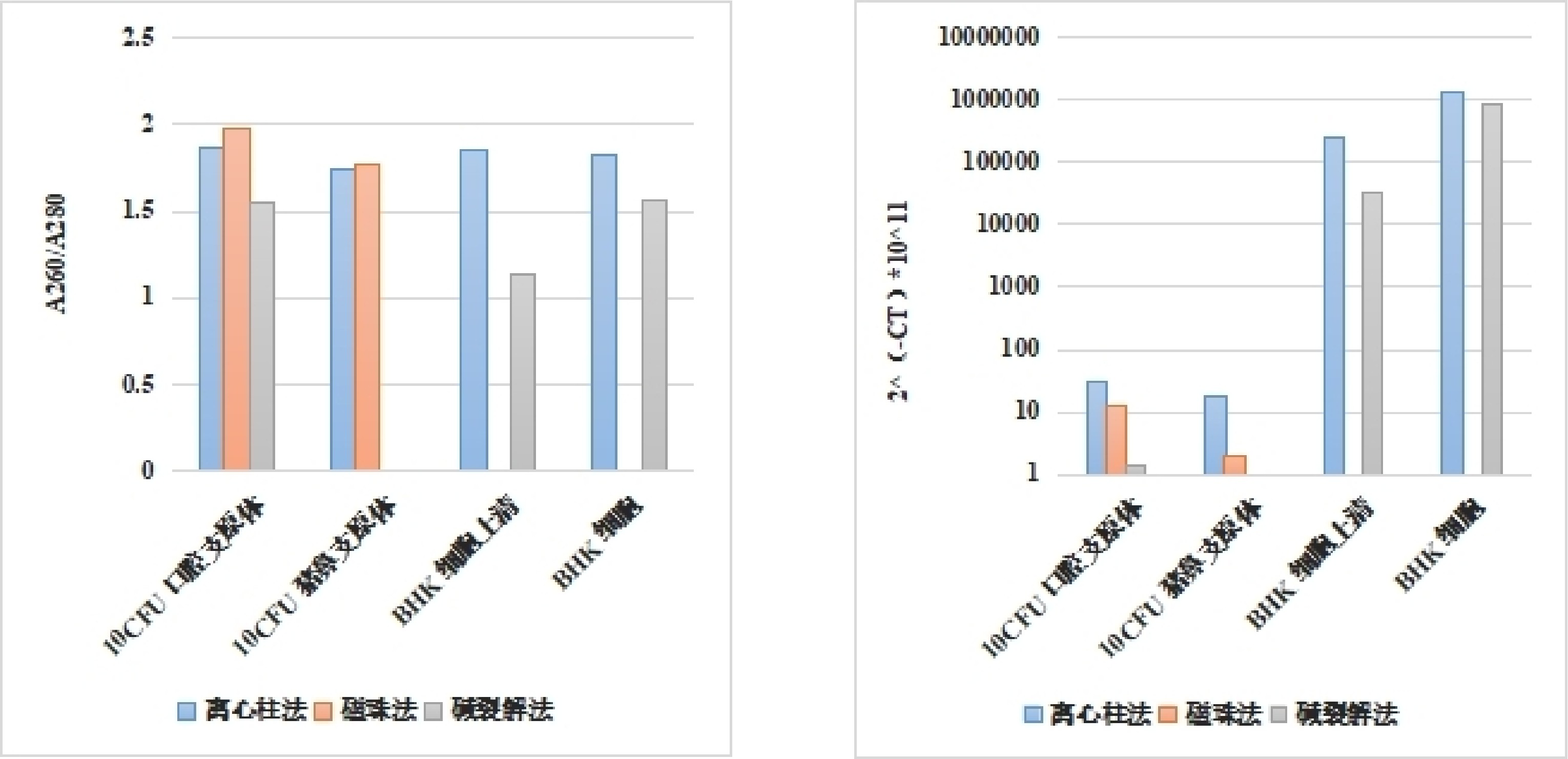
图3-5 不同方法提取四种类型样本DNA纯度比对 图3-6 不同方法提取三种类型样本DNA-qPCR扩增结果
注:在qPCR检测中,CT值越低,代表样本中检测到的目标DNA拷贝数越高,越早检出支原体污染。
实测数据表明:
在纯度(A260/A280)方面,离心柱法基本与本公司磁珠法持平,均符合国标要求,且显著优于碱裂解法,成功规避了有机溶剂残留与杂质抑制风险。
在下游qPCR表现中,离心柱法提取的DNA扩增效果显著优于磁珠法与碱裂解法,可提前约1 ~ 4个循环检出支原体,在微量支原体菌株和高支原体含量的细胞上清中表现更佳,为早筛和高灵敏度检测提供了坚实的物质基础。
04 产品矩阵:支原体DNA提取与检测系列
|
产品名称 |
货号 |
|
支原体基因组DNA提取试剂盒(离心柱法) |
SG-DP050/SG-DP100 |
|
支原体qPCR检测试剂盒说明书(荧光探针法) |
MP-D050T/MP-D100T |
|
支原体检测试剂盒(PCR-膜条法) |
MP-S050T/MP-S100T |
 支原体qPCR试剂盒
支原体qPCR试剂盒
支原体DNA提取试剂盒
05 综合验证:DNA提取试剂盒性能实测
5.1 国标要求验证
按照国标文件GBT+37875-2019:《核酸提取纯化试剂盒质量评价技术规范》,我们对自研的支原体基因组DNA提取试剂盒(离心柱法)进行了规范的产品验证。经验证,该产品纯度、完整性、得率、精密度、再现性与稳定性均符合国标要求。
5.2 样本类型适配性
经验证,该试剂盒适用于多种样本中支原体DNA的提取,包括:贴壁/悬浮细胞培养上清液、细胞沉淀、血清、复杂生物制品等。
5.3 下游应用
针对提取出的DNA是否在下游应用中具备效率与准确性,我们进行了以下验证。
搭配产品:支原体qPCR检测试剂盒(MP-D050T/MP-D100T)。
参考标准:欧洲药典(EP 2.6.7)。
|
|
|
|
|
|
10 CFU/mL口腔支原体 |
24/24 |
|
10 CFU/mL猪鼻支原体 |
24/24 |
|
|
10 CFU/mL肺炎支原体 |
24/24 |
|
|
|
不含支原体的细胞基质 |
未检出 |
|
大肠杆菌 |
未检出 |
|
|
基质效应 |
Vero细胞上清/沉淀+10^6 CCU/mL肺炎支原体 |
回收率:80% - 120% |
|
Hela细胞上清/沉淀+10^6 CCU/mL肺炎支原体 |
||
|
CHO-K1细胞上清+10^6 CCU/mL肺炎支原体 |
||
|
血清+10^6 CCU/mL肺炎支原体 |
结果表明,用该试剂盒提取出的DNA进行qPCR扩增后,灵敏度可达10 CFU/mL,回收率可达80% - 120%,且结果准确特异,提取效率高,符合药典规定。
06 数据实测:比对知名厂家,早筛快人一步
在支原体污染的早期筛查中,培养上清液中游离的微量核酸往往是唯一的线索。为了验证自研支原体DNA提取试剂盒的真实捕获能力,我们选取了一家国内知名厂家专业竞品,在严格均一的样本条件下开展了“背靠背”平行对照实验,
本次测试严格控制在培养了4d的细胞上清场景,使用自制高敏qPCR体系,旨在回答一个核心问题:当污染信号出现时,谁能更早捕捉到危险信号?
表6-1 阴性CHO-K1细胞上清样本提取质量与扩增结果比对
| 浓度(ng/uL) | A260/A280 | qPCR-CT值 | |
| 自研试剂盒 | 6.6 | 1.98 | 无扩增 |
| 知名竞品 | 8.5 | 1.69 | 无扩增 |
表6-2 阳性HELA细胞上清样本质量与扩增结果比对
| 浓度(ng/uL) | A260/A280 | qPCR-CT值 | |
| 自研试剂盒 | 3.0 | 1.87 | 17.47 |
| 知名竞品 | 14.7 | 1.82 | 20.10 |
注:在qPCR检测中,CT值每降低3.32,预计模板量增加10倍。
对比测试结论:
|
赛唐生物 |
竞品厂家 |
|
|
提取质量 |
√ |
× |
|
零假阳性 |
√ |
√ |
|
高灵敏度 |
√ |
× |
|
|
|
|
基础质量过关
在同等样本量下,得率保持一致或略低于竞品,但质量更好,纯度更高。为下游实验提供了良好模板。
零假阳性:安全底线守得住
在阴性CHO-K1细胞上清中,双方均无扩增信号。证明自研试剂盒与竞品一样,具备优秀的抗干扰能力,能有效排除宿主背景噪音,确保检测结果“假阳性”风险为零。
超高灵敏度:微弱信号抓得牢
在阳性HELA细胞上清中,自研试剂盒的CT值比竞品提前了2.63个循环。这意味着自研产品的核酸回收效率是竞品的约6倍,为细胞库安全争取了宝贵的预警时间!
07 结语:工欲善其事,必先利其器
在支原体检测这条路上,从“源头”抓起,方能行稳致远。选择一款经过验证、专为支原体优化的DNA提取试剂盒,不仅是实验成功的开始,更是对生物安全和数据准确性的庄严承诺!
我们的支原体基因组DNA提取试剂盒(离心柱法),凭借更快的检出速率、优异的抗干扰能力及稳定的性能表现,致力于打破进口依赖,为国内生物医药研发提供精准可靠的工具支持。
专业甄选,稳健护航——助力您的细胞培养安全无忧。
往期推文:《支原体“无处遁形”,荧光探针法qPCR检测试剂盒全新就位》
参考文献
[1] Drexler Hans G,and Uphoff Cord C. "Mycoplasma contamination of cell cultures: Incidence, sources, effects, detection, elimination, prevention." Cytotechnology 39.2(2002): 75-90.
[2] European Directorate for the Quality of Medicines & HealthCare (EDQM). European Pharmacopoeia, 11th Ed. Chapter 2.6.7: Mycoplasmas. Strasbourg: EDQM; 2023.
[3] Deutschmann M S ,Kavermann H ,Knack Y .Validation of a NAT-based Mycoplasma assay according European Pharmacopoiea[J]. Biologicals, 2009, 38(2): 238-248.
[4] Wilson I G. Inhibition and Facilitation of Nucleic Acid Amplification[J]. Applied and Environmental Microbiology, 1997, 63(10): 3741-3751.
[5] Boom R S, Sol C J A, Salimans M M M ,et al. Rapid and Simple Method for Purification of Nucleic Acids[J]. Journal of Clinical Microbiology, 1990, 28(3): 495-503.
[6] Tan S C, Yiap B C. DNA, RNA, and Protein Extraction: The Past and The Present[J]. Journal of biomedicine & biotechnology, 2009(Pt.3): 2009.

WEB:www.bluegene.cc
www.cellgenebio.com
E-mail:sales@bluegene.cc
TEL:400-882-6373 / 021-61106433
|
qPCR-CT值 |
|
20.10 |




